截至2023年6月,大气中的CO₂含量已经上升到424 ppm,CO₂的转化与利用迫在眉睫[1]。近年来,电催化CO₂还原的研究已经取得了长足进步,通过电催化方式可以将CO₂转化为CO、HCOOH、CH₄、C₂H₅OH等[2~6]。然而,目前电催化CO₂还原研究仍然无法满足工业化生产的需求,诸多问题有待解决[7]:
1.产物选择性仍然较低,特别是高附加值化学品。较低的选择性将增加产物的分离和纯化难度;
2.目标产物的局部电流密度很低,目标产物所需过电位很高。过低的电流密度和较高的过电位直接影响电催化CO₂还原反应能量转化效率;
3.电催化CO₂还原反应的反应机理有待进一步研究;
4.反应装置仍无法满足工业需求,如电极的耐久性、离子交换膜的性能、催化剂的稳定性等等。

目前实验室中使用的电催化CO₂还原的反应池主要包括H型电解槽(H-Cell)、流动型电解槽(Flow Cell)和膜电极电解槽(Membrane Electrode Assembly,MEA)[8]。
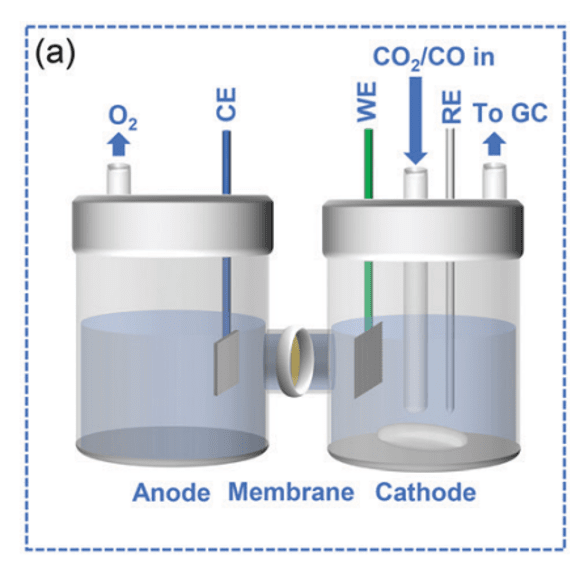
图a. H型电解槽示意图[8].
H型电解槽由阴极室、阳极室和离子交换膜组成。CO₂连续通入到阴极室中,发生还原反应,CO₂携带气体产物进入气相色谱仪检测,阳极室主要发生析氧反应。H型电解槽一般选用0.5 M KHCO₃作为电解液。H型电解槽装置较为简单,成本较低。然而由于CO₂在电解液中有限的溶解度和扩散系数,导致反应传质效率低,反应速率慢。H型电解槽中进行的电催化CO₂还原电流密度一般低于100 mA/cm2 [9]。此外,中性电解液无法有效抑制HER反应的发生。
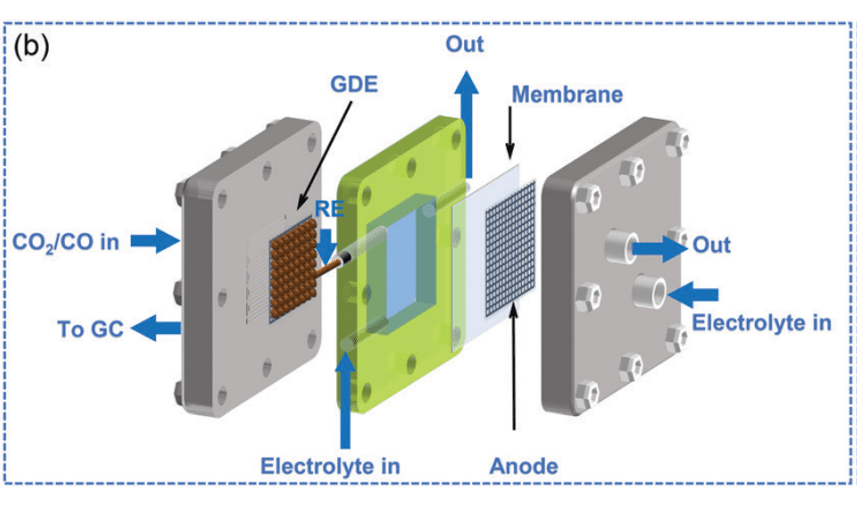
图b. 流动型电解槽示意图[8].
流动型电解槽主要由多孔疏水气体扩散层、阴极室、阳极室和离子交换膜组成。CO₂连续穿过多孔疏水气体扩散层与催化剂和电解液在气-液-固三相界面发生反应,有效解决了H型电解槽传质效率低的问题[10]。同时,流动型电解槽缩短了阴极室和阳极室间的距离,有效降低了电解液的阻抗和整个反应系统的欧姆降[11]。流动型电解槽一般选用1 M KOH作为电解液,可有效抑制HER反应的竞争。流动型电解槽中进行的电催化CO₂还原反应电流密度一般大于500 mA/cm2 [11]。尽管流动型电解槽可以达到较高的电流密度,但其稳定性仍然存在问题。由于气体扩散层的稳定性问题,流动型电解槽存在电解液溢流的隐患。除此之外,CO₂与碱性电解液直接接触容易形成碳酸盐或碳酸氢盐,堵塞气体扩散层的气体传输通道,影响反应速率[9,11]。
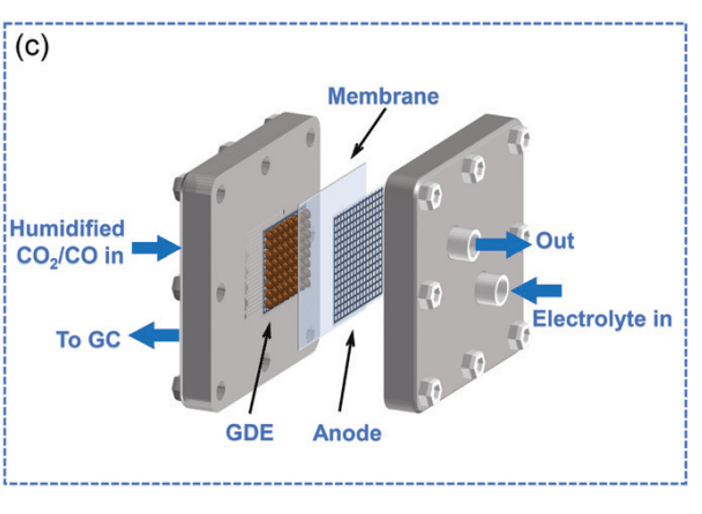
图c. 膜电极电解槽示意图[8].
膜电极电解槽主要由多孔疏水气体扩散层、阴极室、阳极室和离子交换膜组成。膜电极电解槽保留了流动型电解槽传质效率高的优良特点,因此可以达到较高的电流密度。但不同的是,膜电极电解槽的阴极室中没有电解液穿过,一定湿度的CO₂气体穿过多孔疏水气体扩散层直接与催化剂发生气-固相反应,可以有效避免流动型电解槽中存在电解液溢流、气体扩散层堵塞等问题。阳极室中有电解液通过,发生析氧反应,阳极室一般选用一定浓度的KOH作为电解液。由于阴极室中无电解液,参比电极和工作电极之间无法形成电势回路,膜电极电解槽通常为两电极体系,而非三电极体系。这一点不同于H型电解槽和流动型电解槽,双室较短的间距可以显著降低系统阻抗,提高电催化CO₂还原反应速率和能量转化效率[9,10]。然而,膜电极电解槽与实际工业化生产需求仍然存在差距。由于阴极室中没有电解液的循环,还原反应产生的液体产物极易堵塞多孔疏水气体扩散层,影响整个反应的传质。除此之外,离子交换膜的寿命有限,不满足长期生产要求[9]。
除了不断开发新型高效、高稳定性的催化剂之外,新型反应器的设计与研发对于电催化CO₂还原反应研究同样具有重要意义。
为了满足实验需求,泊菲莱科技推出了PLS-MECF系列双室碱性电解槽,其具有高效率、高稳定、长寿命的特性,有PLS-MECF-01双室碱性电解槽和PLS-MECF-02可视化双室碱性电解槽两个型号可选,详细信息可拨打电话400-1161-365咨询或联系在线客服。
以上部分内容是笔者根据参考文献进行翻译和汇总,笔者水平有限,如有错误,请大家指正!
[1] Charles D Keeling, Alane F. Carter, Willem G. Mook, Scripps institution of oceanography[J]. 2023.
[2] Yu Ke, Sun Kainan, Chen Chen* et.al., Oxalate-Assisted synthesis of hollow carbon nanocage with Fe single atoms for electrochemical CO2 reduction [J]. Small, 10.1002/smll.202302611.
[3] Zang Yipeng, Liu Tianfu, Wang Guoxiong* et.al., In situ reconstruction of defect-rich SnO2 through an analogous disproportionation process for CO2 electroreduction[J]. Chemical Engineering Journal, 2022, 5: 446.
[4] Deng Bangwei, Huang Ming, Dong Fan* et.al., The crystal plane is not the key factor for CO2-to-methane electrosynthesis on reconstructed Cu2O microparticles[J]. Angewandte Chemie International Edition, 2021, 61: 7.
[5] Wang Pengtang, Huang Xiaoqing*, Qiao Shizhang* et.al., Boosting electrocatalytic CO2-to-ethanol production via asymmetric C-C coupling[J]. Nature Communications, 2022, 13: 3754.
[6] Mangjeet Chhetri, Che Fanglin*, Yang Ming* et.al., Dual-site catalysts featuring platinum-group-metal atoms on copper shapes boost hydrocarbon formations in electrocatalytic CO2 reduction[J]. Nature Communications, 2023, 14: 3075.
[7] She Xiaojie, Shik Chi Edman Tsang*, Shu Ping Lau* et.al., Challenges and opportunities of electrocatalytic CO2 reduction to chemicals and fuels[J]. Angewandte Chemie International Edition 2022, 22: 49.
[8] Ma Wenchao, Xie Shunji*, Wang Ye* et.al., Electrocatalytic reduction of CO2 and CO to multi-carbon compounds over Cu-based catalysts[J]. Chemical Society Reviews, 2021, 50: 12897.
[9] Yuan Lei, Zeng Shaojuan, Zhang Suojiang* et.al., Advances and challenges of electrolyzers for large-scale CO2 electroreduction[J]. Materials Reports: Energy, 2023, 3. 100177.
[10] Xu Dezhi, Liu Xue*, Ma Tianyi* et.al., Electrocatalytic CO2 reduction towards industrial applications[J]. Carbon Energy, 2023, 15: 230.
[11] Lai Wenchuan, Lin Zhiqun*, Huang Hongwen* et.al., Design strategies for markedly enhancing energy efficiency in the electrocatalytic CO2 reduction reaction[j]. Energy Environ. Sci., 2022, 15: 3603.